厄他培南化学名为(4R,5R,6S)-3-[(3S,5S)-5-[(3-羧基苯基)氨基甲酰基]吡咯烷-3-基]硫-6-(1-羟乙基)-4-甲基-7-氧代-1-氮杂双环[3.2.0]庚-2-烯-2-甲酸,分子式为C22H25N3O7S,其相对分子量为475.51500,密度是1.55 g/cm3。临床上用于治疗复杂性腹腔感染、复杂性皮肤软组织感染、社区获得性肺炎、复杂性尿路感染、急性盆腔感染、严重肠杆菌科细菌感染等。
化合物简介基本信息中文名称:厄他培南
中文别名:(4R,5R,6S)-3-[(3S,5S)-5-[(3-羧基苯基)氨基甲酰基]吡咯烷-3-基]硫-6-(1-羟乙基)-4-甲基-7-氧代-1-氮杂双环[3.2.0]庚-2-烯-2-甲酸;美洛培南母核;
英文名称:ertapenem
英文别名:Ertapenem;AC-6814;(4R,5S,6S)-3-[(3S,5S)-5-[(3-carboxyphenyl)carbamoyl]pyrrolidin-3-yl]sulfanyl-6-[(1R)-1-hydroxyethyl]-4-methyl-7-oxo-1-azabicyclo[3.2.0]hept-2-ene-2-carboxylic acid;UNII-G32F6EID2H;
CAS号:153832-46-3
分子式:C22H25N3O7S
结构式: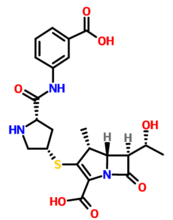
分子量:475.51500
精确质量:475.14100
PSA:181.57000
LogP:1.28040
物化性质密度:1.55 g/cm3
沸点:813.9ºC at 760 mmHg
闪点:446ºC
折射率:1.71
药理毒理该品是一种新型碳青霉烯类抗生素,通过与青霉素结合蛋白(PBP)结合,干扰细菌细胞壁的合成,导致细菌生长繁殖受抑制,少数出现细胞溶解。该品对甲氧西林敏感金葡菌、肺炎链球菌、化脓性链球菌等革兰阳性菌、肠杆菌科细菌具有高度抗菌活性;嗜血杆菌属、卡他莫拉菌、脑膜炎奈瑟球菌等对该品高度敏感,但对甲氧西林耐药葡萄球菌、肠球菌属、铜绿假单胞菌、不动杆菌属等细菌对该品耐药。该品对大多数青霉素酶、头孢菌素酶和超广谱ß-内酰胺酶稳定,但可被金属酶水解。该品对人类肾脱氢肽酶-Ⅰ稳定,不需与西司他丁等联合应用。2
毒理研究遗传毒性:在下列体外试验中,包括碱性洗脱/大鼠肝细胞试验、中国仓鼠卵巢细胞染色体畸变试验、TK6人淋巴母细胞样细胞致突变试验,以及在小鼠体内微核试验中,均未发现厄他培南有致突变活性,也未发现有基因毒性。
生殖毒性:当给小鼠和大鼠静脉注射厄他培南的剂量高达700mg/kg/日时,对交配行为、生殖力、生育力或胚胎存活均无影响。按体表面积计算,给予小鼠的这一剂量大约相当于给予人推荐剂量1g的3倍;按血浆AUCs计算,给予大鼠这一剂量所产生的暴露值大约相当于给予人推荐剂量1g的1.2倍。
当给小鼠和大鼠静脉注射厄他培南的剂量高达700mg/kg/日时,通过对胎儿外表、内脏和骨骼进行检查,未发现发育毒性。按体表面积计算,给予小鼠的这一剂量大约相当于给予人推荐剂量1g的3倍;就血浆AUCs而言,给予大鼠这一剂量所产生的暴露值大约相当于给予人推荐剂量1g的1.2倍。然而,当给予小鼠的剂量达700mg/kg/日时,观察到胎儿的平均体重轻微减少以及骶尾椎骨化数目相应减少。
在大鼠中,厄他培南能通过胎盘屏障。
致癌性:尚未在动物中进行评估厄他培南潜在致癌性的长期研究。3
药代动力学静滴该品0.5g、1g和2g后30min内达血药浓度峰值(Cmax),分别为71.3mg/L、137.0mg/L和255.9mg/L。肌注该品1g后生物利用度约为90 ,达峰时间为2.3h,Cmax为67mg/L。
该品的血浆蛋白结合率为92%~95%,浓度低时蛋白结合率较高。主要经肾脏排出,其血浆半衰期为4.3~4.6h。健康青年志愿者静脉应用同位素标记的该品1g后,尿液和胆汁中药物排除率分别为80%和10%,尿液中药物原形和代谢产物各占40%。2
吸收将厄他培南用符合美国药典标准的1%盐酸利多卡因注射液(溶于生理盐水,不含肾上腺素)溶解,肌肉注射推荐剂量1g后,厄他培南几乎完全被吸收。平均生物利用度约为90%。按每日肌肉注射1g的剂量计算时,达到血浆峰浓度(Cmax)所需的平均时间(Tmax)约为2.3小时。
分布厄他培南能与人的血浆蛋白高度结合,主要是白蛋白。在健康的年轻成人中,当血浆浓度增高时,厄他培南与蛋白的结合则减低,结合率从血浆浓度近似值小于100μg/mL时的95%左右下降至血浆浓度近似值为300μg/mL时的85 %左右。
代谢在健康的年轻成人中,静脉输注1g放射性同位素标记的厄他培南后,血浆中的放射活性主要来自厄他培南(94%)。厄他培南的主要代谢产物是无活性的β-内酰胺环被水解而形成的开环衍生物。用人肝微粒体进行的体外研究表明,厄他培南对细胞色素P450(CYP)6种主要同工酶(1A2、2C9、2C19、2D6、2E1和3A4)所介导的代谢均无抑制作用(参阅药物相互作用)。
体外研究表明,厄他培南对P-糖蛋白介导的地高辛或长春碱的转运无抑制作 用。厄他培南不是P-糖蛋白介导转运的底物(参阅注意事项,药物相互作用)。
清除厄他培南主要通过肾脏清除。在健康年轻成人和13~17 岁的患者中,平均血浆半衰期大约为4 小时,在3 个月~12 岁的儿科患者中平均血浆半衰期约为2.5 小时。
给健康的年轻成人静脉输注放射性同位素标记的厄他培南1g 后,大约80%从尿中排出,其中约38%以原型排泄,37%以开环的代谢产物排泄。另有10%从粪中排出。
给健康年轻成人静脉输注厄他培南1g,在给药后0 至2 小时期间,经尿液排出的厄他培南数量占用药剂量的百分比平均为17.4%,在给药后4 至6 小时期间为5.4%,而在给药后12至24 小时期间为2.4%。
特殊人群**肾功能不全:**在26名伴有不同程度的肾功能损害的成年受试者(年龄31岁~80岁)中研究了厄他培南总体和未结合部分的药代动力学。单次静脉输注厄他培南1g后,未结合药物在轻度肾功能不全病人(Clcr 60-90 mL/min/1.73m)和中度肾功能不全病人(Clcr 31-59mL/min/1.73m)中的AUC分别是健康年轻受试者(年龄25岁~45岁)的1.5倍和2.3倍。对于肌酐清除率≥31mL/min/1.73m的病人无需调整剂量。与健康年轻受试者相比,未结合药物在重度肾功能不全病 人(Clcr 5-30mL/min/1.73m)和终末期肾功能不全病 人(Clcr




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国